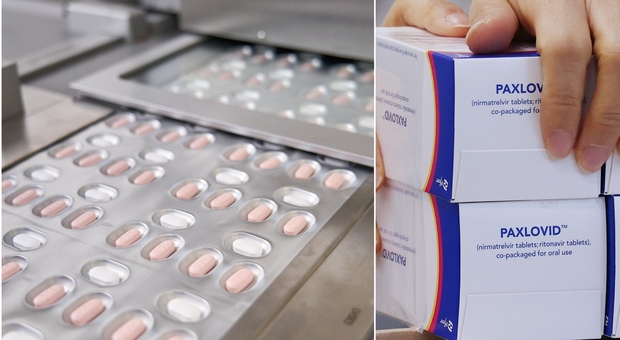
Inizierà oggi la distribuzione alle Regioni e Province autonome dei primi 11.200 trattamenti completi dell'antivirale Paxlovid, nell'ambito del contratto finalizzato lo scorso 27 gennaio della Struttura commissariale con la casa farmaceutica Pfizer, d'intesa con il Ministero della Salute.
Il contratto prevede la fornitura di complessivi 600.000 trattamenti completi nel corso del 2022, i quali verranno progressivamenti distribuiti alle Regioni - non appena disponibili - secondo le indicazioni del Ministero della Salute e dell'Aifa. Tutto questo dopo la firma del contratto tra la struttura del Commissario per l'emergenza Francesco Figliuolo e la casa farmaceutica americana.
IL TRATTAMENTO - Paxlovid, che nello studio registrativo si è dimostrato efficace nel ridurre dell'88% il rischio di ospedalizzazione e morte, è indicato - spiega l'Aifa - per il trattamento di «pazienti adulti con infezione recente da Sars-CoV-2 con malattia lieve-moderata che non necessitano di ossigenoterapia e con condizioni cliniche concomitanti che rappresentino specifici fattori di rischio per lo sviluppo di Covid-19 severo». Il trattamento con Paxlovid deve essere iniziato entro 5 giorni dall'insorgenza dei sintomi e ha una durata di 5 giorni. «Le modalità per la selezione dei pazienti e per la prescrivibilità e distribuzione del farmaco saranno le stesse già stabilite per l'altro antivirale orale (molnupiravir)», informa l'ente regolatorio nella nota. «È previsto l'utilizzo di un Registro di monitoraggio, che sarà accessibile sul sito dell'Agenzia».